Hofmann重排是最古老的以及构建胺的常用合成方法. 但是用于该方法的比较实用的试剂仍然是比较少的. 使用溴的碱性溶液的方法收率不是很令人满意,并且不是很稳定. 因此开发了许多其他的氧化体系,比如高价碘(III)试剂( PhI(OCOCF3)2, PhIO-HC02H, PhI(OTs)OH, and PhI(OAc)2 ); 四乙酸铅; 苄基三甲基三溴化铵; NBS-AgOAc。
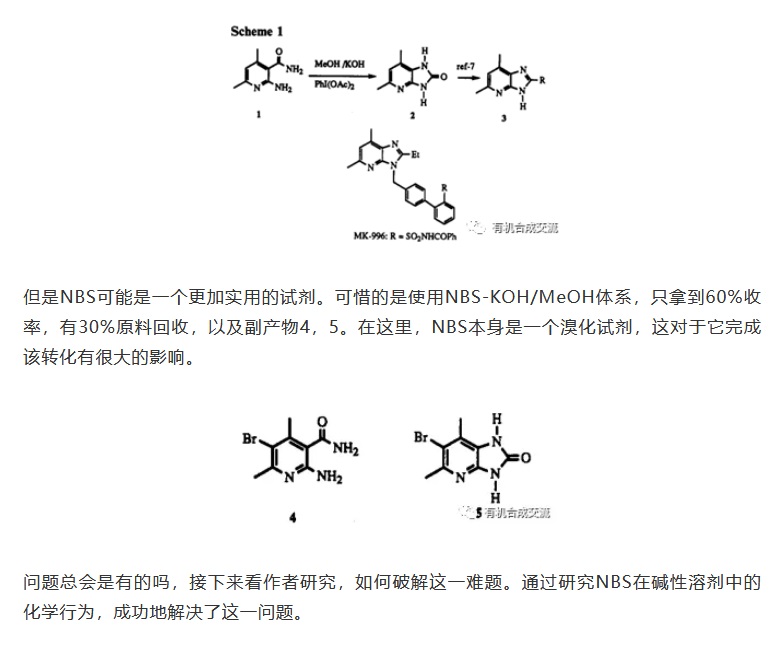
碱在其中起了很大的作用。如果没有KOH, 只能拿到4,没有产物脲生成。加入0.25当量KOH后,发现4减少了,脲2多起来。当使用2.5eq KOH,1eq NBS的时候,最大达到60%转化,并且生成1.1%的4和11.7%的5。很明显,如果没有碱,那么NBS只是一个溴化试剂,但是当有碱存在的时候,NBS就具有了氧化剂的功能。
接下来通过低温NMR进行研究. KOH溶解在氘水里面,冷却到-5°C后,加入NBS。定期取样做1H和13C测试。结果表明,当NBS溶解的时候,已经没有NBS存在了。主要的产物经过鉴定为琥珀酰胺酸二甲盐(8)以及琥珀酰亚胺钾盐(7)。其中转换成7是可逆的,经过时间推移,NBS与7之间的平衡被不可逆转化为8打破。16h后,有96%的8生成了。再增加时间,出现了新的化合物10。经过表征10是8的Hofmann重排产物。
在Hofmann重排中,真正起作用的氧化剂是琥珀酰胺酸二甲盐8。反应结束后通过过滤,得到的化合物NMR表征,确定是琥珀酰胺酸二甲盐。但是想通过往琥珀酰胺酸里面加入Br2/KOH制备盐8并没有成功。它只能通过NBS的开环得到,想用KOBr进行氧化无效。

基本反应进程:酰胺1先被8氧化成N-Br酰胺14,然后重排成异氰酸酯,被分子内氨基捕获,生成产物2。
这篇文献看的非常过瘾,其实这种问题在我们合成的过程中经常碰到,具有很大的普遍性,只不过很多合成人员碰到了,并不当一回事,也不去思考为什么转化不完,导致反应有所缺陷。
学习:
-
知己知彼,百战不殆。这是化学合成永恒的话题,这属于意识问题。很多人瞧不起理论验证,机理研究,图快,不愿意探究。长久发展下去,你除了成为交货工具以外,在理论以及认知上,没有丝毫进步。刚开始你可能比别人快点,但是过一段时间,差距马上缩短,紧接着被反超。磨刀不误砍柴工,有时间的话,多去探究探究下究竟,自己研究下机理,百利而无一害。化学反应有果,其中必有一个因在那里,没有弄清楚因,永远只能被反应牵着鼻子走。
-
NBS的双重特性:溴化试剂和氧化剂。怎么去调控或者将选择性做出来。选择性有时候是通过不同的试剂来调控的,同一个试剂采用不同的操作方式也可以调控选择性。
-
对投料顺序要有充分的认识。这是一个大问题,不是小问题,情况千变万化。最近我们做一个项目PPh3+Br2,生成的中间体也是在温度较高的时候不稳定,如果你及时把原料加进去,中间体一生成就被捕获,就降解的少。中间体的稳定性是有机合成高效与否的一个重点,有机化学讲究匹配,如果中间体生成过快或者过慢,都会对化学反应收率产生巨大影响。中间体生成的速度刚刚好,或者采用措施,降温,加添加剂,加配体等方式稳定住中间体,都可以把反应从很烂做到很好。反应效果差,自己先思考下,中间的中间体是什么?有没有什么办法可以稳定下这个中间体?
-
Hofmann重排制备脲。这是合成脲的一个常见方法。看到脲,可以思考下能不能用此重排来合成。当然这个重排有几种原料可以过来,比如羧酸用curtisus重排,酰胺用Hofmann重排,异羟肟酸酯用Lossen重排。
-
使用氘代试剂开反应,可以研究反应历程。现在有各种各样的氘代试剂,直接用氘代试剂做反应,进行NMR跟踪,可以获得很多信息。
-
机理这种东西,你多做一些反应,它可能可以提供一些奇奇怪怪的数据。很多时候,人为控制的数据都不是好数据,客观做出来的奇怪数据可能对机理解释效果更大,更能打你脸~~。所以多去收集数据,不会有错。
原文:J. Am. Chem. Soc. 1994, 11 6, 7947-7948

