有机反应沿着不同的反应历程会得到不同的产物,如果反应还未达成平衡前就分离产物,利用各种产物生成速率差异来控制产物分布称动力学控制反应,其主要产物称动力学控制产物。
如果让反应体系达成平衡后再分离产物,利用各种产物热稳定性差异来控制产物分布称热力学控制反应或平衡控制反应,其主要产物称热力学控制产物。
两种控制的区别是在分离产物时反应体系是否达到平衡态,而此概念中并没有涉及反应条件, 反应条件不同只是通过影响在分离产物时反应体系离化学平衡态的距离而影响反应产物的分布。
要利用控制因素不同,而控制不同的主要产物,并不是任何平行反应都行,而是应当满足一定条件的反应才有可能。下面以A 分别生成B 和C 两种产物为例:
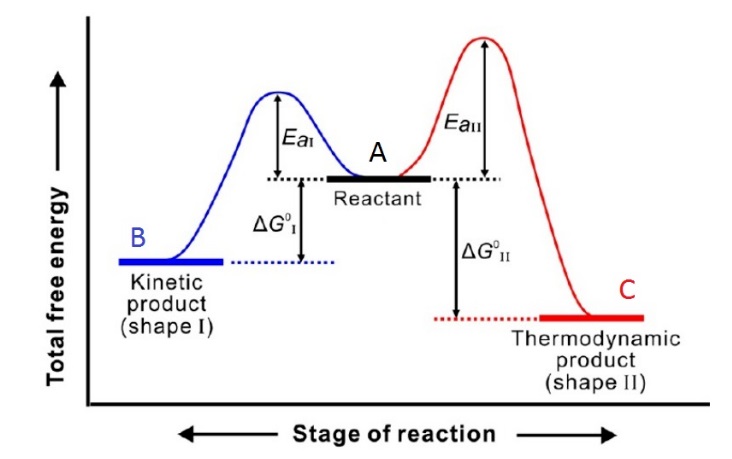
首先是两个方向均有明显的可逆性,如果两个方向的反应几乎没有可逆性,B、C 一旦生成就不能逆转,直到反应物消耗完为止,很明显生成速度快者量最多,它就是主要产物,平衡也无从谈起,则产物都为动力学控制产物。
其二, 两种不同产物之间有较明显的热稳定性差异,如上图所示,如C 的热稳定性明显比B高, 且热稳定性相对较好的C产物,生成反应有较高的活化能,当然它的生成反应速率较低,而热稳定性相对较低的B,生成反应却有较低的活化能,相应B有较高的生成反应速率。【根据阿伦尼乌斯公式: k=Ae-Ea/RT (指数式)。k为速率常数,R为摩尔气体常量,T为热力学温度,Ea为表观活化能,A为指前因子(也称频率因子),活化能Ea越小,反应速率常数越大】
第三,有的反应还应当在一定的温度范围内进行。同样根据阿伦尼乌斯公式: k=Ae-Ea/RT 。增加温度可以减小活化能的影响,因此,增加温度有利于得到热力学产物;降低温度,有利于得到动力学产物
在反应达到平衡前分离产物,无论什么温度范围内,始终有生成B产物的速率,大于生成C产物的速率,只是随着温度的升高两者的差异减小, 因此在任意温度下进行反应,都有反应未达成平衡就分离产物,反应受动力学控制— C 产物为主要产物。
若达成平衡后才分离产物,反应受热力控制— C产物为主要产物。在后一种情况下,两直线有一交点,设其对应温度为T,反应在低于T的温度范围内进行时,生成B的速率大于生成C产物的速率,仍然是反应受动力学控制时,B 产物为主要产物,而反应受热力学控制时,C 产物为主要产物。当温度等于T 时,生成产物B 和C 的速率相等,所以反应体系离平衡尚远时产物中B、C 比例几乎相同,达成平衡后,C产物为主要产物。当温度高于T时,生成C产物的速率大于生成B产物的速率,C产物就既是热力学稳定产物,也是生成速率快的产物,无论是热力学控制产物,还是动力学控制产物,C产物均是主要产物。从热力学方面:要使热力学稳定性较高的C产物在平衡产物中为主要产物,同样对温度有一定的限制,如果各种产物的平衡表达式形式相同,那么各种产物的平衡浓度与其平衡常数成正比例关系。
在有机化学中,绝大多数反应是动力学控制的。也有很多涉及动力学和热力学控制竞争的例子。例如羟醛缩合反应用NaOH这种弱碱会生成更稳定的化合物。主要产物为热力学更稳定的产物,动力学控制的反应通常设计低温,强(路易斯)酸强(路易斯)碱的条件,LDA拔氢条件下,会拔掉位阻最小(动力学上最容易接近)的氢生成烯醇负离子中间体,然后进攻另一个羰基,得到的反应结果很可能与NaOH条件下的不同;1,3-丁二烯与氯化氢的加成反应,1,2-加成产物为动力学控制产物,1,4-加成产物为热力学控制产物;甲苯的磺化反应,邻对位取代的比例控制;萘的磺化反应,α,β异构体的比例控制。
一、百度百科:https://baike.baidu.com/item/%E7%83%AD%E5%8A%9B%E5%AD%A6%E6%8E%A7%E5%88%B6/7200451?fr=aladdin


